Le terme d’angiome a été de longue date utilisé à la fois pour les lésions vasculaires tumorales et malformatives. On utilise actuellement plus volontiers le terme d’anomalies vasculaires
On reconnaît actuellement deux groupes d’anomalies vasculaires :
- les tumeurs vasculaires, l’hémangiome du nourrisson étant la tumeur la plus fréquente ;
- les malformations vasculaires de type capillaire, veineux ou lymphatique qui sont à flux lent, et de type artériel ou artérioveineux à flux rapide.
Les conséquences cliniques et la prise en charge en matière de diagnostic comme de traitement, sont tout à fait spécifiques à chaque groupe.
RETENTISSEMENT PHYSIQUE ET PSYCHIQUE
Quel que soit le type d’anomalie vasculaire, il altère, plus ou moins selon son siège et sa gravité, l’apparence et l’esthétique, et parfois, il perturbe une fonction ou il est source de douleurs. S’il s’agit d’une malformation vasculaire complexe, le plus souvent un traitement radical n’est pas possible, cet aspect est à aborder clairement avec le malade et sa famille au cours des consultations.
Le vécu des patients et de leur famille doit être pris en compte aujourd’hui avec plus d’acuité, car, sentiments de peur, perte, deuil, stigmatisation sociale, perte d’anonymat dans la foule, grief et insatisfaction dans la prise en charge sont couramment exprimés.
INFORMATION AUX MALADES
L’annonce du diagnostic, et du handicap à en attendre, constitue une étape essentielle qui doit être faite dans les meilleures conditions. Nombre de patients et de parents cherchant des renseignements sur internet sont mal orientés par un mot clé erroné, ou se perdent dans un forum aux discussions angoissantes : ils vivent des affres inutiles,
Il est inutile de faire une multitude d’examens vasculaires si un diagnostic clinique précis est évoqué et qu’il n’y a pas de possibilités ou de demande thérapeutiques immédiates.
Le risque éventuel de transmission héréditaire d’une anomalie vasculaire inquiète les familles et doit être évoqué ; certaines lésions sont pour nous si évidemment sporadiques, accidentelles, que cela n’est souvent même pas abordé au cours de la consultation.
Le diagnostic prénatal des lésions vasculaires développées in utero est aujourd’hui régulièrement fait
TUMEURS VASCULAIRES
3.1 – HÉMANGIOME DU NOURRISSON
STRATÉGIE DE SURVEILLANCE
L’hémangiome infantile est la plus fréquente des tumeurs du nourrisson, avec une incidence de 1 à 10 p. 100.
L’hémangiome est plus fréquent chez les filles, les nourrissons à peau blanche et chez les prématurés de moins de 1 500g. Il semble apparaître en peau saine, mais dans 50 p. 100 des cas il est prévisible dès la naissance sous la forme d’une lésion prémonitoire à type de macules rouges parsemées de télangiectasies ou de taches blanches « anémiques » de vasoconstriction. Ces précurseurs permettent de prédire la surface finale qu’occupera l’hémangiome mais pas son volume ni son épaisseur.
La phase de prolifération dure quelques mois, rarement plus de six à huit. Elle est suivie d’une très lente régression spontanée, terminée entre 5 et 10 ans, plus ou moins vite, en fonction de la taille et du volume qu’avait atteint la lésion.
Celle-ci restitue une peau normale ou laisse des séquelles à type de peau flasque, d’anétodermie, de dyschromie, de télangiectasies, de résidu fibro-adipeux, ou de déformations structurales. Les séquelles sont d’autant plus importantes que l’hémangiome a été plus volumineux.
— le plus banal est l’hémangiome superficiel, souvent appelé « tubéreux », dont la taille va de quelques millimètres à plusieurs centimètres. La couleur rouge rutilante et l’aspect irrégulier de « fraise » permettent le diagnostic.
— un autre aspect, plus rare, correspond à l’hémangiome profond, dermique, hypodermique, sous une peau de couleur normale ou bleutée.
— enfin, l’hémangiome mixte superpose les deux aspects.
Plus de 80 p. 100 des hémangiomes sont petits (moins de 2 cm). Mais certains atteignent une surface et une épaisseur considérables.
Des localisations particulières telles que l’orbite, le nez, la bouche, la parotide, le sein, le périnée, etc. sont particulièrement à risques de séquelles.
Plus un hémangiome est important, et plus il s’agit de filles : l’incidence relative passe de 3 filles pour 1 garçon dans les formes banales, à environ à 9 filles pour 1 garçon au moins pour les formes segmentaires étendues et compliquées.
En matière de diagnostic, quand faut-il faire des examens complémentaires ? Rarement en fait. Le Doppler couleur, dans les mains d’un opérateur averti, fait le diagnostic d’hémangiome devant une masse sous-cutanée chaude et dense, évocatrice car riche de vaisseaux artériels et veineux. Le scanner avec injection de produit de contraste iodé est un examen non seulement irradiant (à éviter si possible chez le nourrisson) mais aussi moins performant que l’IRM. Scanner et IRM recherchent une extension profonde, en particulier dans des formes péri-oculaires ou parotidiennes
Au niveau céphalique, les hémangiomes de forme focale (3/4 des cas) sont localisées sur les proéminences, sont arrondis, de taille variable, et 60 p. 100 d’entre eux siègent dans la région centrofaciale.
Les formes en plaques dites segmentaires (1/4 des cas au visage) ont onze fois plus de risques que les formes dites focales de faire une complication (volume important, ulcération, association à des hémangiomes viscéraux, ou à des anomalies malformatives)
Ce sont ces formes qui justifient le plus d’examens complémentaires.
Les hémangiomes segmentaires faciaux :
- S1 (fronto-palpébro-temporal),
- S2 (maxillaire),
- S3 (mandibulaires)
- S4 (centro-facial, en triangle inversé sur le front, triangle dont la pointe inférieure peut s’étendre de la glabelle au nez et à la lèvre supérieure).
Les malformations associées à certains de ces hémangiomes constituent le syndrome PHACES, regroupant des anomalies de la fosse Postérieure, un Hémangiome céphalique en règle segmentaire et souvent peu épais, des anomalies Artérielles, Cardiaques, oculaires (Eye) et Sternales.
Un bilan neuroradiologique par IRM et ARM s’impose chez tout nouveau-né qui développe un vaste hémangiome facial, tout particulièrement si celui-ci couvre les régions frontopalpébrale et centrofaciale (S1+S4).
OUTILS DU TRAITEMENT
En fonction de la gravité clinique, de l’évolutivité et du siège plusieurs options thérapeutiques pourront se discuter :
— abstention et « laisser faire la nature » tout en surveillant l’évolution ;
— traiter avec des médicaments par voie orale ou systémique ;
— proposer un traitement chirurgical soit en phase précoce de prolifération, soit au stade tardif de séquelles cutanées et d’éventuelles séquelles structurales au visage surtout ;
— utiliser des lasers médicaux.
STRATÉGIE THÉRAPEUTIQUE
QUI TRAITER ?
Pendant la phase de poussée, environ 15 à 20 p. 100 des enfants porteurs d’hémangiomes vont être traités, parce que leur lésion s’étale sur une large surface et/ou devient volumineuse. Le plus souvent, le traitement médical démarre entre 1 et 3 mois.
COMMENT TRAITER ?
Les outils thérapeutiques sont multiples : médicaments, lasers et chirurgie, et une combinaison des techniques peut s’avérer utile
Les outils thérapeutiques :
– Les bétabloquants, en particulier le propranolol, sont devenus ces dernières années le traitement médical de première ligne des hémangiomes compliqués
– Les corticoïdes sont, maintenant donnés seulement en seconde intention
– L’interféron a 2a ou 2b
– Les traitements topiques comme les dermocorticoïdes puissants ou d’imiquimod, n’ont pas vraiment fait la preuve d’un intérêt thérapeutique réel dans les hémangiomes. De plus en plus de publications signalent l’efficacité des bétabloquants locaux, timolol et propranolol,
– Le laser pulsé appliqué en début de prolifération est peu efficace, il paraît accélérer la régression de la composante superficielle, mais est sans effet sur les composantes profondes d’hémangiomes mixtes. En revanche, les lasers sont utiles en fin de régression pour effacer des télangiectasies résiduelles. Le resurfaçage à l’aide d’un laser CO2, d’un laser Erbium YAG, ou d’un laser fractionné peut améliorer une peau laissée cicatricielle et dyschromique après régression.
3.2 – HÉMANGIOME CONGÉNITAL
Ils sont pleinement développés in utero et s’avèrent pour certains rapidement résolutif en moins de 14 mois après la naissance (RICH) alors que d’autres persisteront indéfiniment (NICH).
- le RICH (Rapidly Involuting Congenital Hemangioma) par définition subit une résorption post-natale spontanée et rapide.
L’aspect le plus typique du RICH est une plaque bombée ou une masse ovoïde, saillante, rosée ou pourpre, télangiectasique au centre et cernée d’un halo pâle, très souvent localisée sur les membres ou sur la tête autour de l’oreille. Cette forme est facile à reconnaître et elle régresse bien, en laissant soit une aire d’atrophie, soit une nappe télangiectasique rosée plane.
- NICH (Non-Involuting Congenital Hemangioma) ne régresse absolument pas.
Le NICH apparaît dès la naissance comme une plaque ronde ou ovale, bien limitée, rosée ou violacée, télangiectasique, avec cerne blanc bleuté, et quelques veines de drainage équatoriales. Des microfistules artérioveineuses peuvent y être détectées. La lésion ne régresse jamais, elle persiste inchangée suivant la croissance corporelle, ou elle s’aggrave légèrement.
3.3 – AUTRES TUMEURS VASCULAIRES
- L’ angiome en touffes(AT, encore appelé angioblastome) est une tumeur vasculaire cutanée, apparaissant à tout âge, mais surtout chez le nourrisson.
- L’ hémangioendothéliome kaposiforme (HEK) est également soit congénital soit acquis.
- Le syndrome de Kasabach-Merrittne complique pas un hémangiome infantile.
4 – MALFORMATIONS VASCULAIRES
4.1 – MALFORMATIONS CAPILLAIRES
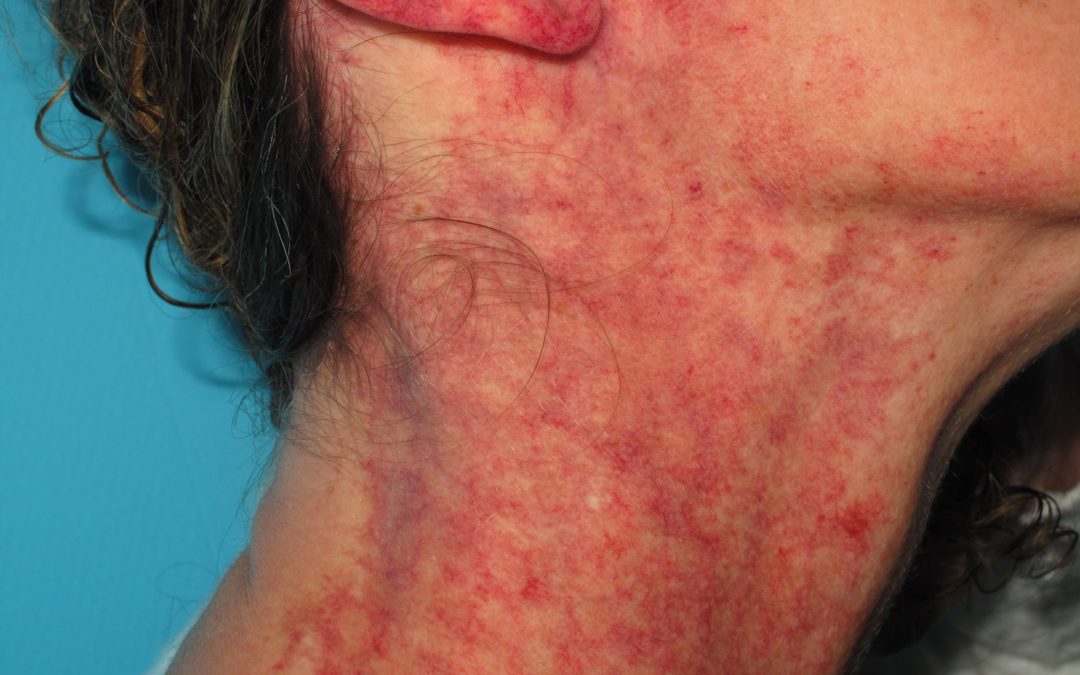
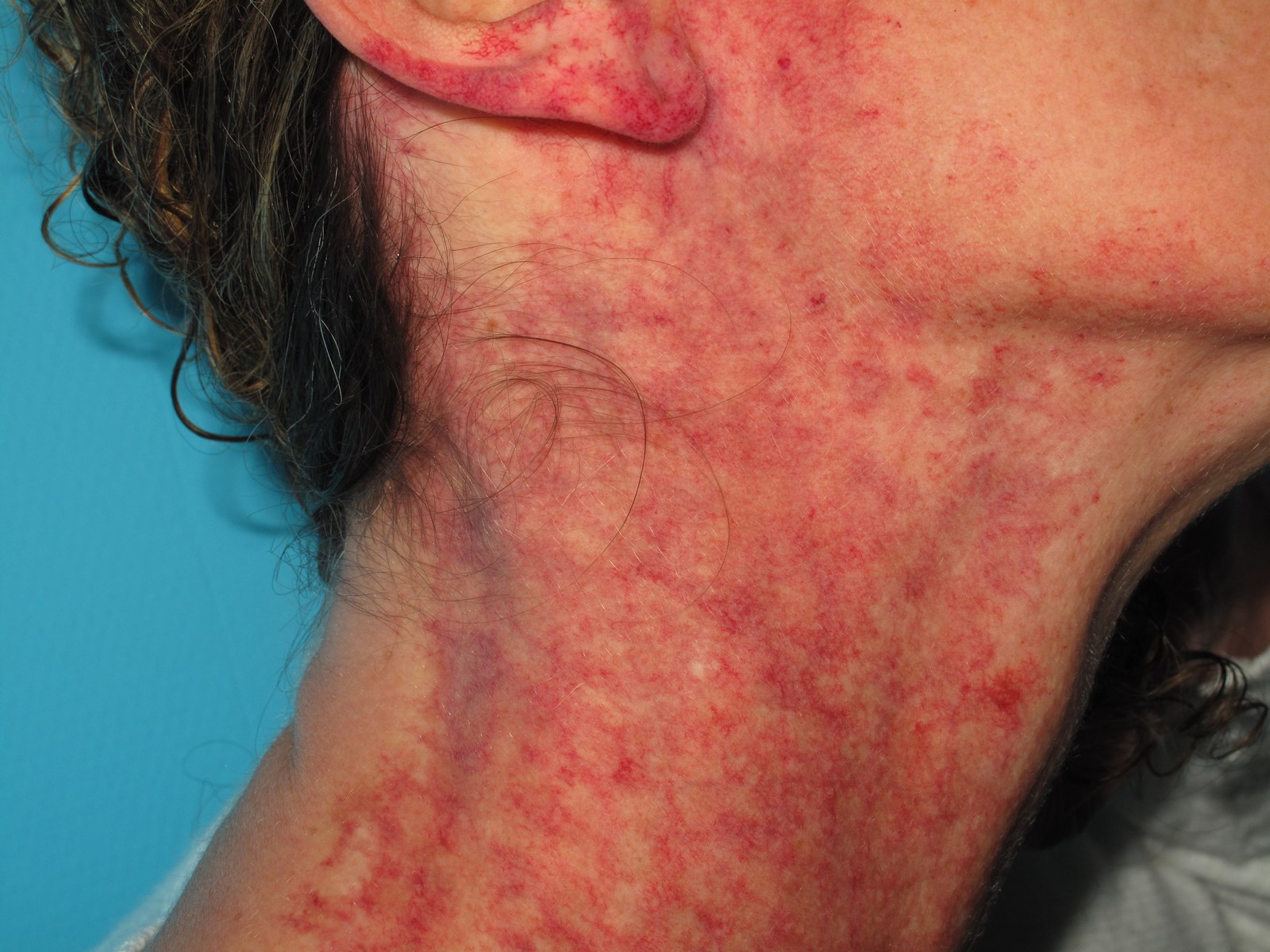
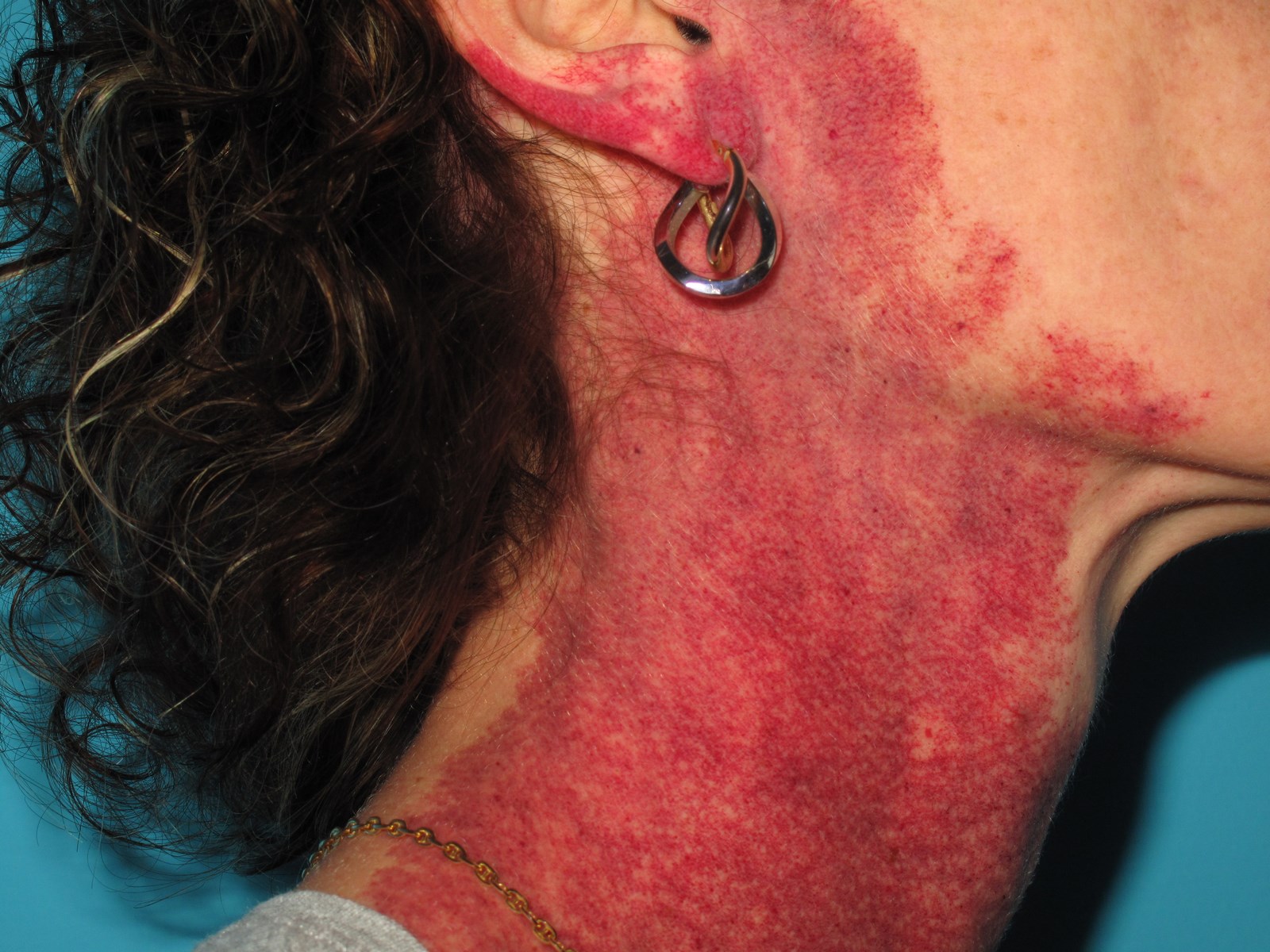
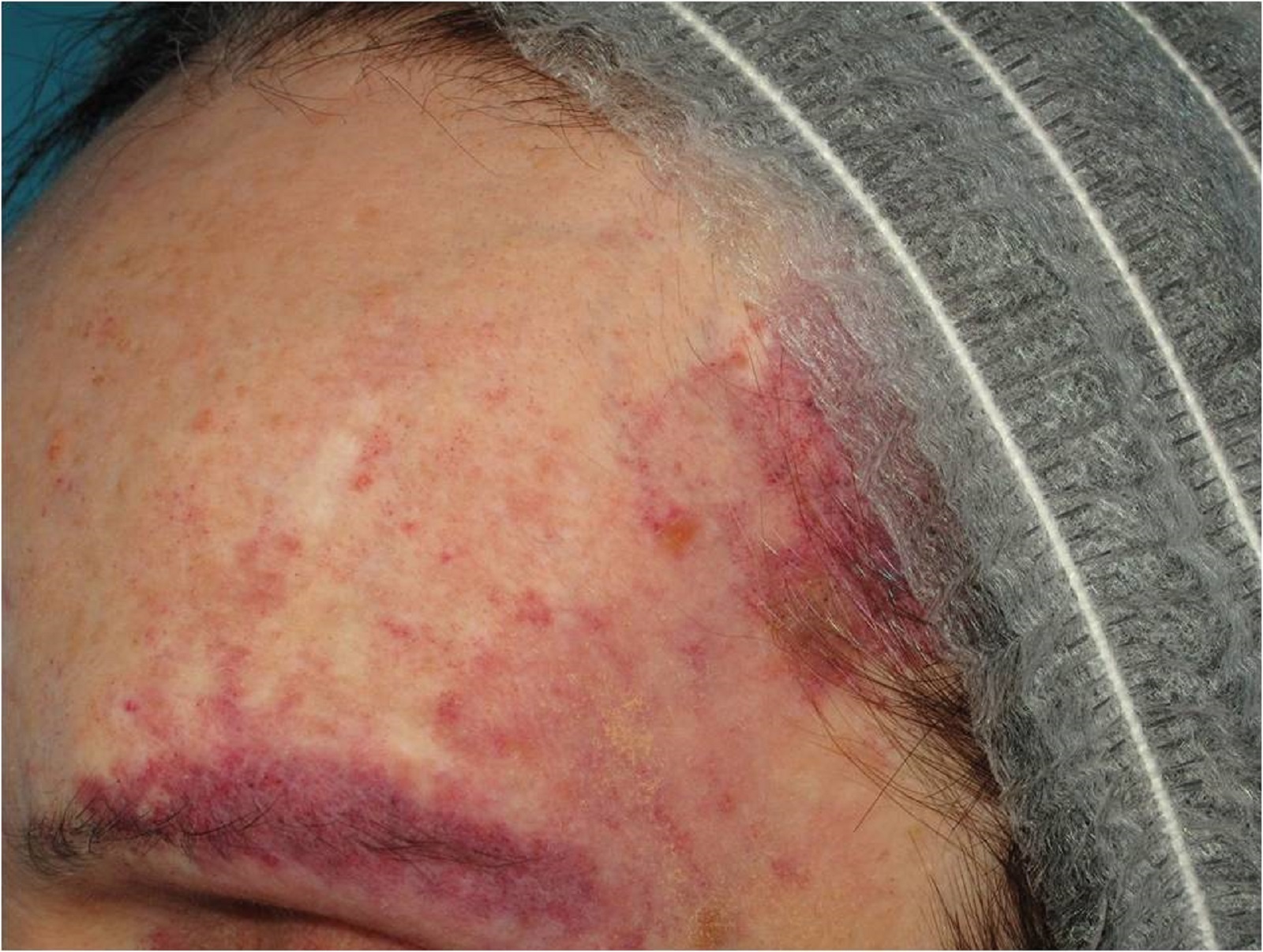
Elles sont représentées par l’angiome plan et les télangiectasies. L’angiome plan siège n’importe où, il peut s’étendre aux muqueuses.
STRATÉGIE DE SURVEILLANCE
L’angiome plan est de taille et de coloration variables, du rose pâle au rouge chez l’enfant (classique « tache de vin »), il est présent dès la naissance. La coloration peut s’estomper légèrement le premier mois de vie, puis elle va le plus souvent foncer très progressivement vers la couleur lie-de-vin (port-wine stain des Anglo-Saxons). Au visage, la peau est d’épaisseur normale chez l’enfant mais peut épaissir avec l’âge ; en outre, des nodules saillants peuvent se développer en surface, masquant le caractère « plan » de la lésion initiale, ce qui peut égarer le diagnostic. Dans certains cas, l’angiome plan facial est associé à une hypertrophie des tissus mous ou osseux sous-jacents (angiome plan hypertrophique). Ce caractère hypertrophique est fréquent en particulier avec les angiomes plans des régions labiales, gingivales et maxillaire.
OUTILS DU TRAITEMENT
La malformation capillaire elle-même est traitée aujourd’hui grâce aux lasers pulsés. Les syndromes d’hypertrophie faciale (tissus mous et maxillaires) relèvent de la chirurgie d’harmonisation
Traiter le plus tôt possible dans la vie un nourrisson porteur d’angiome plan est souhaitable, car la nappe d’angiome plan suivra la croissance corporelle de l’enfant, augmentant la surface à balayer. De plus, comme signalé précédemment, la peau peut s’épaissir et la coloration de l’angiome s’intensifier après la puberté.
4.2 – MALFORMATIONS LYMPHATIQUES
Elles sont la conséquence d’anomalies de développement du système lymphatique : kystes, dilatation de collecteurs lymphatiques et agénésie d’autres vaisseaux sont observés
OUTILS DU TRAITEMENT
On dispose de deux possibilités, la chirurgie d’exérèse et la sclérothérapie percutanée à l’aide de divers sclérosants injectés dans les poches lymphatiques
4.3 – MALFORMATIONS VEINEUSES
Elles sont liées à une anomalie des parois veineuses, sorte d’incapacité à stabiliser leur taille, ce qui explique l’expansion et la lente aggravation, toute la vie. La plupart sont sporadiques, il y a seulement 1 à 2 p. 100 de formes familiales.
STRATÉGIE DE SURVEILLANCE
Cliniquement, les malformations veineuses se traduisent par une tuméfaction molle, compressible, sous une peau qui, si elle est envahie jusque dans le derme papillaire, est nettement bleue. La température locale est normale. La lésion augmente de volume avec l’élévation de la pression veineuse locale en position déclive, lors d’effort physique, de cris ou pleurs, et elle s’affaisse en situation inverse.
OUTILS DU TRAITEMENT
Deux types de traitement sont possibles : scléroses par injection intralésionnelle et/ou traitement chirurgical.